[편집자주] 파이낸스스코프는 단독성 기사, 인사이트 등을 담은 내용을 유료로 제공하고 있습니다. 유료 출고시 제목은 '프리미엄 회원에게만 제공되는 기사입니다'로 표시되고 제목은 본문에 제공합니다. 또한 무료로 전환시 기사의 제목을 재배치하고 공개됩니다.
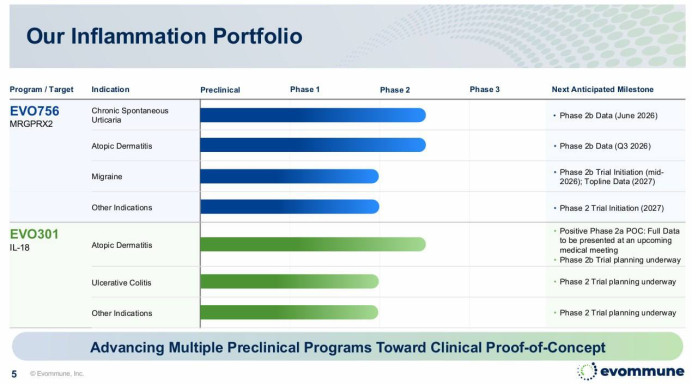
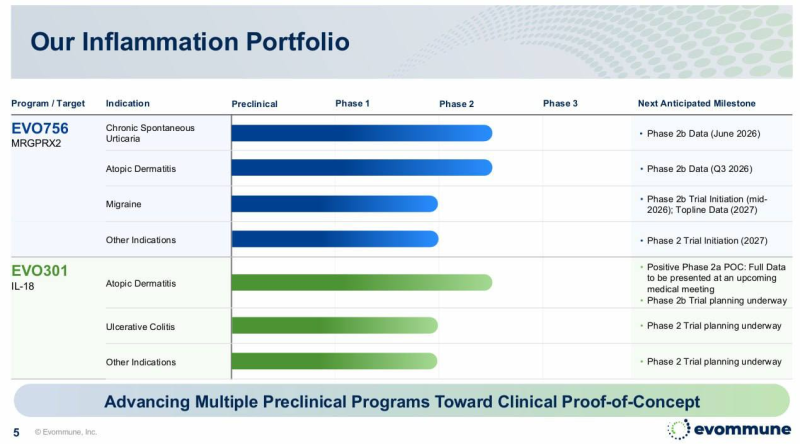
에보뮨(Evommune)이 에이프릴바이오에서 도입한 IL-18 BP 신약 후보물질 'EVO301(APB-R3)'의 적응증을 확대한다.
해당 에셋은 지난 2024년 에보뮨이 에이프릴바이오로부터 4억7500만달러 규모로 글로벌 권리를 도입한 약물이다.
에보뮨이 적극적으로 적응증 확장에 나서는 만큼 에이프릴바이오에도 시장의 관심이 주목되고 있다. 만약 4번째 적응증으로 확대할 경우에는 별도의 계약금을 에이프릴바이오에 지급해야 한다.
에보뮨은 7일(현지시간) 1분기 실적발표를 통해 이같은 내용을 밝혔다.
EVO301은 IL-18BP을 타깃하는 약물로 에이프릴바이오의 반감기 증대 플랫폼 SAFA 기술이 적용됐다. 기존 단일항체 약물 대비 염증조직의 분포 효율성을 개선할 수 있을 것으로 기대된다.
에보뮨은 EVO301의 고농도 피하투여(SC) 제형 개발을 완료하고 제조단계에 진입했다. 내년 중반에는 아토피피부염 임상2b상을 개시할 계획이다.
추가 적응증 확장도 검토한다. 이전까지 아토피피부염 외에 궤양성대장염(UC)을 확정한 상태였다. 이날 에보뮨은 심혈관 관련 염증성 질환, 식품 알레르기(food allergy) 등에 대해서도 임상2상 진입 가능성을 검토하고 있다고 설명했다. 이와함께 홈페이지의 파이프라인 정보도 업데이트했다.
에보뮨은 오는 13~16일 시카고에서 열리는 SID 2026(Society For Investigative Dermatology
)에서 아토피피부염 치료 내 IL-18 억제 기전 및 EVO301의 차별성과 관련된 전임상 결과를 발표할 예정이다.